בשנים האחרונות תרופות ממשפחת GLP-1 הפכו לאחד הנושאים המרכזיים ברפואה. הן פותחו תחילה לטיפול בסוכרת מסוג 2. בהמשך התברר כי הן יעילות מאוד גם בטיפול בהשמנה. כעת מתברר כי ייתכן שהשפעתן רחבה אף יותר.
מאמר חדש שפורסם בשנת 2026 ב Nature Communications מציג מנגנון ביולוגי מסקרן. לפי החוקרים, הורמון GLP-1 אינו רק מפחית תיאבון ומשפר את חילוף החומרים. הוא עשוי גם להגן על הלב לאחר התקף לב. ההשפעה מתרחשת דרך כלי הדם הזעירים שמזינים את שריר הלב.
לממצא זה עשויה להיות משמעות גדולה. אם המנגנון יתורגם לטיפול קליני, תרופות ממשפחת GLP-1 עשויות לשפר את זרימת הדם ללב לאחר אירוע איסכמי. בכך הן עשויות לצמצם את הנזק לשריר הלב ולסייע בתהליך השיקום.
כאשר אדם עובר התקף לב, אחד הטיפולים החשובים ביותר הוא פתיחת העורק החסום באמצעות צנתור דחוף. פעולה זו מחזירה את זרימת הדם בעורק הכלילי הראשי. אך לעיתים הסיפור אינו מסתיים שם.
גם לאחר פתיחת העורק הגדול, הדם לא תמיד מצליח להגיע לכלי הדם הזעירים בתוך שריר הלב. כלי דם מיקרוסקופיים אלה עלולים להישאר חסומים. מצב זה נקרא תופעת No-Reflow.
למרות שהעורק נפתח והזרימה בו חוזרת, חלקים מרקמת הלב אינם מקבלים אספקת דם וחמצן מספקת. התופעה אינה נדירה. היא מתרחשת בכמחצית מהמטופלים לאחר פתיחת העורק החסום.
כאשר No-Reflow מתרחש, הנזק לשריר הלב עלול להיות גדול יותר. התוצאה יכולה להיות ירידה בתפקוד הלב, אוטם גדול יותר, עלייה בסיכון לאי-ספיקת לב ואף עלייה בתמותה.
לכן הבנת המנגנון שמוביל לחסימה של כלי הדם הזעירים הפכה לאחד האתגרים המרכזיים בקרדיולוגיה המודרנית. החוקרים מחפשים דרכים לשפר את זרימת הדם גם ברמת המיקרו-סירקולציה של הלב.
מי סוגר את כלי הדם הזעירים? תאי הפריציטים
המחקר החדש התמקד בתאים מיוחדים הנקראים פריציטים (Pericytes). אלו תאים זעירים העוטפים את הנימים, כלי הדם הקטנים ביותר בגוף.
הפריציטים פועלים כמו שרירים מיקרוסקופיים של מערכת הדם. הם מסוגלים להתכווץ ולהתרפות. כך הם שולטים בקוטר הנימים ובכמות הדם שזורמת דרכם.
כאשר מתרחשת איסכמיה, כלומר מצב שבו רקמת הלב סובלת מחוסר חמצן, הפריציטים מתכווצים. הכיווץ מצר את הנימים ומקטין את זרימת הדם.
הבעיה היא שבמקרים רבים הכיווץ הזה אינו חולף גם לאחר פתיחת העורק הראשי בצנתור. למרות שהזרימה בעורק הגדול חוזרת, הנימים עצמם נשארים צרים ולעיתים חסומים. לכן חלקים משריר הלב ממשיכים לקבל פחות דם וחמצן.
במודלים ניסיוניים נמצא כי לאחר אירוע איסכמי קוטר הנימים באזור הפריציטים מצטמצם בכ־45%. במקביל שיעור הנימים החסומים עולה בצורה חדה, מכ־12% במצב תקין לכ־74% לאחר האיסכמיה.
נתונים אלה ממחישים עד כמה התכווצות הפריציטים יכולה לפגוע בזרימת הדם בתוך שריר הלב. גם לאחר פתיחת העורק הכלילי הראשי, זרימת הדם ברמה המיקרווסקולרית עלולה להישאר מוגבלת.
GLP-1 מפעיל מנגנון הגנה חדש בלב
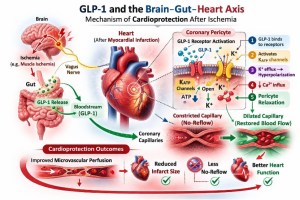
החוקרים מצאו כי ההורמון GLP-1 מסוגל להרפות את תאי הפריציטים ולפתוח מחדש את הנימים הזעירים בלב. כאשר הנימים מתרחבים, זרימת הדם ברשת המיקרוסקולרית של כלי הדם משתפרת. כך הדם מצליח להגיע טוב יותר לרקמת הלב גם לאחר אירוע איסכמי.
המנגנון מתרחש בכמה שלבים ביולוגיים ברורים. תחילה GLP-1 נקשר לרצפטורים הנמצאים על פני תאי הפריציטים. הקישור מפעיל תעלות אשלגן מיוחדות בתא הנקראות KATP channels. כאשר התעלות נפתחות, יוני אשלגן יוצאים מהתא.
יציאת האשלגן גורמת להיפרפולריזציה של ממברנת התא. תהליך זה מפחית את כניסת הסידן לתא. כאשר ריכוז הסידן יורד, תאי הפריציטים נרפים.
הרפיית הפריציטים מאפשרת לנימים שסביבם להתרחב. כתוצאה מכך ההתנגדות לזרימת הדם פוחתת וזרימת הדם בתוך שריר הלב משתפרת. הדם יכול להגיע לאזורים שנפגעו מהאיסכמיה ולהזין את הרקמה.
החוקרים הדגימו גם עד כמה המנגנון הזה חיוני. כאשר חסמו את רצפטור GLP-1 או את תעלות האשלגן מסוג KATP, האפקט המגן נעלם לחלוטין. הנימים נותרו מכווצים וזרימת הדם לא השתפרה.
הממצאים מחזקים את ההבנה כי GLP-1 אינו פועל רק על תחושת הרעב או על חילוף החומרים, אלא עשוי להשפיע ישירות גם על מערכת כלי הדם של הלב.
ציר חדש בגוף: מוח – מעי – לב
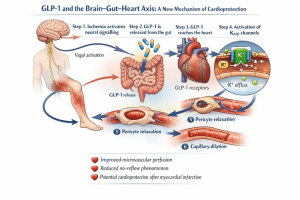
אחד הממצאים המרתקים במחקר הוא גילוי של מסלול תקשורת ביולוגי בין איברים שונים בגוף. החוקרים מצאו כי כאשר מתרחשת איסכמיה באיבר מסוים, למשל בשרירי הגפיים, מופעל מנגנון עצבי דרך עצב הואגוס. זהו אחד העצבים המרכזיים במערכת העצבים האוטונומית.
הפעלת העצב מובילה לשחרור ההורמון GLP-1 מתאי המעי. ההורמון נכנס לזרם הדם, נישא ברחבי הגוף ומגיע אל הלב.
כאשר GLP-1 מגיע ללב, הוא מפעיל מנגנונים ביולוגיים שעשויים להגן על שריר הלב מפני נזק איסכמי. כך הגוף מפעיל מערכת הגנה פנימית בתגובה למחסור בחמצן.
הממצאים מצביעים על קיומו של ציר תקשורת חדש בין איברים שונים בגוף: המוח, המעי והלב. במסגרת ציר זה פועלות יחד מערכת העצבים, מערכת העיכול ומערכת הלב וכלי הדם.
שיתוף הפעולה בין המערכות מאפשר הפעלה של מנגנון הגנה טבעי. מנגנון זה מסייע לשמור על זרימת הדם לשריר הלב ולצמצם את הנזק לאחר אירוע איסכמי.
החוקרים מכנים מנגנון זה Brain-Gut-Heart Signaling Pathway – מסלול איתות ביולוגי המחבר בין המוח, המעי והלב.
למה זה חשוב מבחינה קלינית?
בשנים האחרונות הצטברו עדויות ממחקרים קליניים גדולים לכך שתרופות ממשפחת GLP-1 מפחיתות אירועים קרדיווסקולריים משמעותיים. מטופלים המקבלים תרופות אלו מראים ירידה בשיעור התקפי הלב, שבץ ותמותה קרדיווסקולרית. אולם עד לאחרונה לא היה ברור לחלוטין מהו המנגנון הביולוגי שמסביר את ההשפעה המגינה הזו.
המחקר החדש מציע הסבר אפשרי וחשוב. לפי הממצאים, תרופות ממשפחת GLP-1 אינן פועלות רק דרך ירידה במשקל, שיפור רמות הסוכר או הפחתת דלקת. ייתכן שהן משפיעות גם ישירות על כלי הדם הזעירים בלב ומשפרות את זרימת הדם המיקרוסקולרית לאחר אירוע איסכמי.
אם מנגנון זה אכן פועל גם בבני אדם, המשמעות הקלינית עשויה להיות רחבה: זרימת דם טובה יותר לנימי הלב עשויה להפחית את גודל האוטם לאחר התקף לב, לשפר את תפקוד שריר הלב ולצמצם את הסיכון להתפתחות אי-ספיקת לב בהמשך. בסופו של דבר, השפעה זו עשויה גם לשפר את שיעורי ההישרדות לאחר אירוע לבבי.
השלכות לעתיד: פיתוח תרופות ממוקדות
בשנים האחרונות הצטברו עדויות ממחקרים קליניים גדולים לכך שתרופות ממשפחת GLP-1 מפחיתות אירועים קרדיווסקולריים משמעותיים. מטופלים שמקבלים תרופות אלו מציגים ירידה בשיעור התקפי הלב, שבץ ותמותה קרדיווסקולרית. עם זאת, עד לאחרונה לא היה ברור לחלוטין מהו המנגנון הביולוגי שמסביר את ההשפעה המגינה הזו.
המחקר החדש מציע הסבר אפשרי וחשוב. לפי הממצאים, תרופות ממשפחת GLP-1 אינן פועלות רק דרך ירידה במשקל, שיפור רמות הסוכר או הפחתת דלקת. ייתכן שהן משפיעות גם ישירות על כלי הדם הזעירים בלב ומשפרות את זרימת הדם המיקרוסקולרית לאחר אירוע איסכמי.
אם מנגנון זה אכן פועל גם בבני אדם, המשמעות הקלינית עשויה להיות רחבה. זרימת דם טובה יותר לנימי הלב עשויה להפחית את גודל האוטם לאחר התקף לב ולסייע בשימור רקמת שריר הלב.
בנוסף, שיפור זרימת הדם עשוי לשפר את תפקוד הלב לאחר האירוע ולצמצם את הסיכון להתפתחות אי-ספיקת לב בהמשך.
בסופו של דבר, השפעה זו עשויה גם לשפר את שיעורי ההישרדות לאחר אירוע לבבי ולהפוך את תרופות GLP-1 לכלי חשוב לא רק בטיפול בהשמנה ובסוכרת, אלא גם בהגנה על הלב.
מעבר להרזיה: פרדיגמה חדשה ברפואה
במשך שנים נתפסו תרופות ממשפחת GLP-1 בעיקר ככלי לטיפול בסוכרת ובהשמנה. הן נועדו לשפר את איזון הסוכר, להפחית תיאבון ולסייע בירידה במשקל. אך בשנים האחרונות מצטברים מחקרים שמצביעים על תמונה רחבה הרבה יותר.
כיום מתברר כי ייתכן שמדובר במשפחה תרופתית בעלת השפעה מערכתית עמוקה. התרופות אינן פועלות רק במסלול אחד. הן משפיעות על כמה מנגנונים ביולוגיים במקביל.
מעבר להשפעה המטבולית, התרופות עשויות לשפר את חילוף החומרים, להפחית תהליכים דלקתיים ולהעניק הגנה למערכת הלב וכלי הדם. בנוסף, הן עשויות להשפיע גם על כלי הדם המיקרוסקולריים ולשפר את זרימת הדם ברקמות.
המחקר החדש מוסיף נדבך חשוב להבנת מנגנוני ההגנה של הלב. הוא מדגים כיצד מערכות שונות בגוף אינן פועלות בנפרד. הן פועלות כחלק מרשת מורכבת של תקשורת בין איברים.
דרך צירי איתות ביולוגיים המחברים בין המוח, המעי והלב, הגוף מפעיל מנגנוני הגנה מתוחכמים. מנגנונים אלה מסייעים להתמודד עם מצבי סטרס ואיסכמיה ולשמור על תפקוד הלב.
מראה מקום




